Độ tan của một chất trong nước, công thức và cách học
Trong hóa học cấp 2, bạn sẽ học về khái niệm độ tan của các chất trong nước. Một số chất sẽ hòa tan trong nước, nhưng những chất khác thì không. Đồng thời, khả năng hòa tan của các chất sẽ không giống nhau. Vậy làm thế nào để xác định đó có phải là chất tan hay không và cách tính độ tan của một chất trong nước như thế nào? Hãy cùng tìm hiểu.
Khả năng hòa tan của các chất trong nước
Độ tan là số gam một chất hòa tan trong nước và tạo ra dung dịch bão hòa ở nhiệt độ môi trường.
Độ hòa tan của một chất trong nước cũng là độ hòa tan của chất đó. Điều kiện là trong dung dịch nước 100 mg, nhiệt độ không đổi, và khi không thể tiếp tục nữa, chúng tạo thành dung dịch bão hòa.
Tuy nhiên, như đã đề cập ở trên, không phải tất cả các chất đều hòa tan trong nước. Vậy làm cách nào để xác định độ tan của một chất? Các nhà khoa học đã đưa ra 3 yếu tố cụ thể sau đây để giúp chúng ta dễ dàng xác định độ tan trong nước của một chất. Tất cả trộn với 100g nước.
- Nếu một chất có thể hòa tan & gt; 10g thì nó là chất tan hay còn gọi là chất hòa tan.
- Một chất ít tan nếu nó có độ tan <1 g.
- Nếu chất chỉ tan
- 0,01g chất không tan.
Tích số tan và tan là hai khái niệm hoàn toàn khác nhau. Tích số tan là tích của nồng độ các ion tự do trong dung dịch bão hòa ở nhiệt độ xác định và chỉ số ion trong phân tử.
Bạn đang xem: Tính tan trong nước là tính chất gì
& gt; & gt; Đăng ký lớp học thử miễn phí môn hóa học từ lớp 8 đến lớp 12
Độ hòa tan của hợp chất trong nước
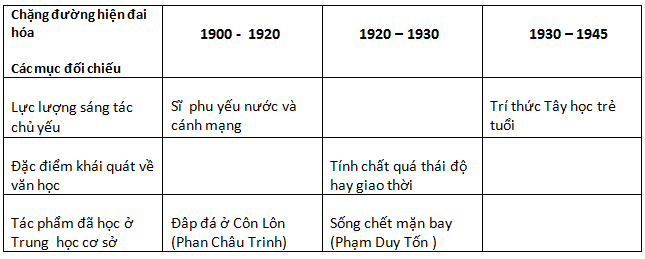
Sau đây sẽ là khả năng hòa tan của các nhóm chất trong nước:
- Bazơ: Hầu hết bazơ không tan. Ngoại trừ nah, koh, ba (oh) 2.
- Axit: Hầu hết các axit đều hòa tan trong nước, ngoại trừ h2 và sio3.
- Muối: Nitrat hòa tan trong nước.
- Ngoài agcl, pbso4, baso4, hầu hết các clorua và sunfat cũng hòa tan.
- Ngoại trừ na2co3 và k2co3, các muối cacbonat về cơ bản là không tan.
Công thức tính tan của các chất trong nước
Công thức tính độ tan của một chất trong nước như sau:
s = (mct / mdm) x100
Vị trí:
- mct là khối lượng của chất tan
- mdm là khối lượng của dung môi
- s là độ hòa tan
Một chất có độ hòa tan càng lớn thì chất đó càng dễ hòa tan trong dung dịch nước 100 mg và ngược lại. Từ công thức trên, chúng ta có thể suy ra mối quan hệ giữa độ tan của một chất và nồng độ phần trăm của dung dịch bão hòa. Công thức cụ thể như sau:
c = (100 giây / (100 + s))
Một số yếu tố ảnh hưởng đến khả năng hòa tan của các chất trong nước
Khả năng hòa tan của một chất trong nước bị ảnh hưởng bởi các yếu tố cơ bản sau:
- Nhiệt độ ảnh hưởng đến độ tan của chất rắn: khi nhiệt độ tăng thì độ tan của chất rắn cũng giảm và ngược lại.
- Ảnh hưởng của chất khí đến độ tan với nhiệt độ và áp suất: Khi nhiệt độ và áp suất cao, chất khí ít tan hơn và ngược lại.
Một số dạng bài tập về tính tan
Sau đây là một số bài tập liên quan đến tính tan của các chất trong nước và các giải pháp của chúng.
Bảng 1: Tính lượng tinh thể ngậm nước cần thêm vào dung dịch
Đối với dạng bài tập này, chúng tôi có các giải pháp sau:
Tính toán theo định luật bảo toàn khối lượng:
(m_ {ddtt} = m_ {tt} + m_ {ddbd})
Vị trí:
- (m_ {ddtt}) là khối lượng của dung dịch tạo thành
- m_ {tt} là khối lượng của tinh thể
- (m_ {ddbd}) là các giải pháp hàng loạt ban đầu
Sau khi có kết quả, tiếp tục áp dụng công thức tính thể tích chất tan trong dung dịch:
(m = m_ {ctcttt} + m_ {ctctddbd})
Vị trí:
- (m_ {ctcttt}) là khối lượng của chất tan có trong tinh thể
- (m_ {ctctddbd}) là chất tan có trong dung dịch ban đầu.
Bảng 2: Lượng chất tan được loại bỏ hoặc thêm vào để tính toán sự thay đổi nhiệt độ
Giải pháp cho các bài tập như sau:
Bước 1: Tính khối lượng dung môi và chất tan có trong dung dịch bão hòa ở nhiệt độ (t_ {1})
Bước 2: Gọi a (g) là khối lượng của chất tan a tìm được sau khi thay đổi nhiệt độ.
Bước 3: Tính lượng dung môi và chất tan có trong dung dịch bão hòa ở (t_ {2})
Bước 4: Áp dụng công thức tính độ tan hoặc c% trong dung dịch bão hòa để tìm ẩn a.
& gt; & gt; Cách vượt qua nỗi sợ hóa học – toppy
Một số bài tập củng cố
Nhiệm vụ 1. Chọn câu trả lời đúng
Ở nhiệt độ nhất định, độ tan của một chất trong nước là:
- Số gam chất có thể hòa tan trong 100 gam dung dịch
- Số gam chất có thể hòa tan trong 100 gam nước.
- Số gam chất đó có thể tan trong 100 gam nước.
- Hòa tan trong 100 g dung môi để tạo thành dung dịch bão hòa.
d. Số gam chất có thể hòa tan trong 100 gam nước để tạo thành dung dịch bão hòa.
Câu trả lời: d đúng.
Bài 2. Độ hòa tan của chất rắn trong nước khi nhiệt độ tăng dần
- Tất cả đều tăng
- Tất cả đều giảm
- Hầu hết đều tăng
- Hầu hết đều giảm
- Không tăng cũng không giảm.
Câu trả lời: c đúng
Bài học thứ ba. Khi giảm nhiệt độ và tăng áp suất, độ tan của chất khí trong nước:
- cả hai đều tăng
- cả hai đều giảm
- có thể tăng hoặc giảm
- không tăng cũng không giảm.
Câu trả lời: a đúng
Bài 4. Dựa vào giản đồ độ tan của chất rắn trong nước (hình 6.5), ta được biết các muối nano3, kbr, kno3, nh4cl, nacl, na2so4 ở nhiệt độ 10oc và 60oc.
Trả lời:
Bắt đầu từ các điểm ở nhiệt độ 10oc và 60oc, chúng ta vẽ các đường song song với trục hòa tan (trục tung), và tại giao điểm của các đường này với đồ thị, chúng ta vẽ các đường song song với nhiệt độ (trục tung). mức độ) chúng ta sẽ đọc khả năng hòa tan của chất như sau:
+ Độ hòa tan nano3: 80g cho 10oc, 130g cho 60oc
+ Độ hòa tan kbr: 60g cho 10oc, 95g cho 60oc
+ Độ tan của hà thủ ô3: 20g đương quy 10oc, 110g dung dịch 60oc
+ Tính tan nh4cl: 30g cho 10oc, 70g cho 60oc
+ độ tan nacl: 10oc 35 g, 60oc 38 g
+ Độ tan của na2so4: 60g cho 10oc, 45g cho 60oc

Trên đây là khái niệm, công thức tính và cách giải của chất tan trong nước. Hi vọng sẽ giúp các bạn học môn hóa hiệu quả.
Xem thêm:
- Chuỗi hoạt động Hóa học Tất cả Kim loại Cấp 9
- Tính chất hóa học của phi kim loại – Ghi chú học tập
- Tính chất hóa học của axit – Học tập Hóa học 9
Giải pháp toàn diện giúp con bạn đạt 9-10 dễ dàng với toppy
Lấy học sinh làm trung tâm, toppy tập trung vào việc tạo ra các lộ trình học tập được cá nhân hóa cho học sinh, giúp học sinh nắm vững kiến thức cơ bản và tiếp thu kiến thức nâng cao với sự trợ giúp của hệ thống nhắc nhở học tập, thư viện thực hành và các đề kiểm tra chuẩn hóa từ 9 đến 10.
Thư viện phong phú
Thư viện video bài giảng với hình ảnh minh họa sinh động và dễ hiểu nhằm thu hút học sinh tham gia vào các hoạt động tự học. Ngân hàng bài tập, đề kiểm tra phong phú, các bài tập tự học được sắp xếp hợp lý. Tự học, tự sửa giúp nâng cao hiệu quả, rút ngắn thời gian học. Kết hợp phòng thi ảo (thi thử) với giám khảo thật để luyện thi IELTS và giải tỏa lo lắng.
Nền tảng học tập thông minh không giới hạn, cam kết hiệu quả
Tất cả những gì bạn cần là điện thoại di động hoặc máy tính / máy tính xách tay có thể học mọi lúc, mọi nơi. 100% học viên trải nghiệm quá trình tự học qua toppy đều đạt kết quả như mong đợi. Các kỹ năng đòi hỏi sự tập trung được cải thiện một cách hiệu quả. Làm lại bài kiểm tra miễn phí cho đến khi bạn vượt qua!
Tự động đặt lộ trình học tập tối ưu
Cung cấp lộ trình học tập cá nhân hóa cho từng học sinh dựa trên các kỳ thi đầu vào, hạnh kiểm học tập, kết quả thực hành của từng đơn vị kiến thức (tốc độ, điểm số); sau đó tập trung vào các kỹ năng và kiến thức còn yếu mà học sinh chưa có.
Trợ lý ảo và cố vấn học tập trực tuyến hỗ trợ bạn trong suốt quá trình học tập
Kết hợp các ứng dụng nhắc nhở bạn học tập, đánh giá học tập thông minh, chi tiết và nhóm hỗ trợ hỏi đáp 24/7 để giúp kèm cặp và động viên học sinh trong suốt quá trình học tập, giúp phụ huynh yên tâm.